Жизненные процессы в человеческом организме во многом зависят от того, чем мы питаемся. Рациональное питание - это ежедневное включение в меню оптимального соотношения жиров, углеводов и белков. Как влияют эти вещества на физические и психические параметры тела? Попробуем разобраться.
Человеческий организм - это 60% воды, 1% углеводов, 19,6% белков и 14,7% жиров.
Белки представляют собой высокомолекулярные органические соединения. Это строительный материал для клеток. Они в организме выполняют целый ряд функций:
- Опорная. Белки являются компонентом костной и хрящевой ткани.
- Транспортная. Она заключается в переносе к органам питательных веществ и кислорода.
- Ферментативная. Это ускорение химических реакций.
- Защитная. Когда в организм человека попадают токсины, белки вступают с ними в реакцию и затем выводятся из тела.
- Генетическая. Это передача наследственных особенностей, свойств.
- Энергетическая. При дефиците энергии в организме белки разрушаются и восполняют этот недостаток.
Если в организме человека вышеуказанных веществ не хватает, то начинает ухудшаться память, слабеет щитовидная железа, нарушаются процессы кроветворения, снижаются функции половых желез и надпочечников.
Попадая в организм, белки перевариваются до аминокислот. Они и поступают в нашу кровь. Более полезными и многофункциональными являются белки животного происхождения. Богатыми их источниками служат рыба, мясо, сыр, яйца, молочные продукты. Норма потребления белка в день для здорового человека составляет полтора грамма на килограмм массы тела. Жиры - главные источники энергии нашего организма. И хотя считается, что эти вещества вредны в наш век гиподинамии, но их роль для человека огромная. Дефицит жиров приводит к снижению усвояемости белков и углеводов, результатом чего будет нарушение обмена веществ. В человеческий организм жиры поступают из двух видов жирных кислот - насыщенных и ненасыщенных. Биологические свойства первых невысокие. Они, к тому же, негативно влияют на работу печени и жировой обмен, способствуют повышению уровня холестерина в крови. А именно он является причиной развития атеросклероза.
Ненасыщенные кислоты - жизненно важные вещества, принимающие участие в обмене жира и холестерина. Этот вид жирных кислот повышает эластичность кровеносных сосудов, снижает их проницаемость. Источниками ненасыщенных жирных кислот являются морская рыба, оливковое, . Богаты ними и . Вредными для организма являются жиры, содержащиеся в сливочном масле, говяжьем жире, сале. Для человека нормой суточного потребления является 90-110 граммов жира.
Углеводы - это тоже богатые источники человеческой энергии. По сравнению с жирами, они гораздо полезнее. Эти вещества на 58% покрывают все энергетические затраты организма. Углеводы могут откладываться про запас, создавая энергетические депо. Поступая в избыточном количестве в организм, углеводы откладываются в печени, мышцах в виде гликогена. Это животный крахмал, способный при нужде расщепляться до состояния глюкозы и в таком виде поступать в ткани. Если же углеводов в пище слишком много, то они могут трансформироваться в жиры.
Еще одна важная функция этих веществ - пластическая. Они принимают участие в строении молекул РНК, АТФ, ДНК. Углеводами являются сахароза, глюкоза, крахмал, фруктоза, целлюлоза, клетчатка. Последняя мало используется организмом. Для человека нормой суточного употребления является 500 граммов углеводов. Если же человек тяжело работает физически или умственно, то этот показатель составляет 700 граммов. Богатыми источниками таких веществ, как углеводы, являются картофель, хлеб, молоко, макаронные изделия. А вот полезными - крупы, овощи, ягоды, фрукты.
Практическая работа по химии:
«Идентификация органических соединений.
Разнообразие и свойства белков, жиров, углеводов»
ученицы 10-А класса
УВК ОШ 1-2 ступеней – МТЛ
Колмычек Анастасии
Цель работы: углубление и закрепление знаний об органических веществах, относящихся к классам белков (протеинов), жиров и углеводов; развитие организационных, технических и интеллектуальных умений учащихся; воспитание интереса к химическому эксперименту и к самостоятельному получению знаний.
С правилами техники безопасности ознакомлена и обязуюсь выполнять!
Жиры
Жиры – это гидрофобные соединения, относящиеся к группе липидов; являются сложными эфирами глицерина и высших жирных кислот. Насыщенные (твердые) жиры содержатся в мясе, сале, креветках, яйцах (желток), молоке, шоколаде, сыре, в кокосовом и сливочном масле. Ненасыщенные (жидкие) жиры содержатся в мясе птицы, рыбы, в оливках, миндале, грецких орехах. А также в подсолнечном, льняном, оливковом, соевом и арахисовом масле.
Оборудование и реактивы: бумажные салфетки, сливочное масло, растительное масло, 2-3 семечки, пипетка, ложечка, несколько стеклянных баночек, вода, медицинский спирт, ацетон, бензин, сувенирные эфирные масла, фотоаппарат.
Опыт № 1
В данных продуктах содержатся жиры, поэтому на салфетках появились жирные пятна. В семечках и маслах содержатся растительные и животные жиры.
Свойства жиров: вязкие жидкости или твердые вещества, легче воды, не имеют четко выраженной температуры плавления; не растворяются в воде, но растворяются во многих органических растворителях. Жиры легко окисляются под воздействием различных факторов: кислорода, температуры, света, ферментов. Прогоркшие жиры имеют неприятный запах, их цвет меняется, ухудшаются органолептические свойства. Чем больше в состав жира входит насыщенных жирных кислот, тем труднее он расщепляется в организме пищеварительными ферментами. Твердые жиры состоят из триглицеридов предельных кислот (пальмитиновой C 15 H 31 СООН, стеариновой C 17 H 35 СООН), а жидкие – из триглицеридов непредельных кислот (олеиновой C 17 H 33 СООН, линоленовой C 15 H 29 СООН).
CH2-O-CO-C17H35
I
CH-O-CO-C17H35
I
CH2-O-CO-C17H35
Тристеарат (твердый)
CH2-O-CO-C17H33
I
CH-O-CO-C17H33
I
CH2-O-CO-C17H33
Триолеат (жидкий)
Опыт № 2
Наблюдения доказали свойства жиров: хорошо растворяются во многих полярных и неполярных растворителях (эфирах, бензине, хлороформе), ограниченно растворяются в спиртах, нерастворимы в воде.
Опыт № 3
Эфирные масла – пахучая смесь жидких летучих веществ, выделенных из растительных материалов. В состав этих веществ входят терпены, кетоны, эфиры, альдегиды и др. Бывают разные эфирные масла. Например, пихтовое, сосновое, розовое, шалфейное, лавандовое, цитрусовое, а также масло ромашки и жасмина.
Эфирные масла широко используются в медицине. Они обладают широчайшим спектром биологической активности, проявляют бактерицидные, противовоспалительные, мочегонные и отхаркивающие свойства.
Пахучие свойства эфирных масел определяют преимущественное использование их для создания ароматных композиций. Состав этих композиций часто очень сложен. Важнейшими современными направлениями запаха в парфюмерии являются цветочный (так называемых белых цветов), «восточный», овощной и их комбинации. Эфирное масло иланг-иланга получают из свежих цветов, собранных летом, методом водной или паровой дистилляции, в несколько этапов.
После первого этапа получается сорт Extra или Bourbon – высший сорт эфирного масла иланг-иланга, весьма популярный и ценимый в парфюмерии.
Углеводы (сахара)
Углеводы – это органические соединения, состоящие из трех элементов – карбона, гидрогена, оксигена. Моносахариды и дисахариды (глюкоза, фруктоза, сахароза) имеют сладкий вкус и растворимы в воде. Полисахариды (крахмал, целлюлоза) обладают другими свойствами. Углеводы – мощный энергетический источник обеспечения жизнедеятельности организмов. Углеводы широко распространены в природе.
Оборудование и реактивы: сахароза, картофельный крахмал, спиртовой раствор йода, пипетка, ложечка, несколько стеклянных банок, вода, электрочайник, кусочек белого хлеба, фотоаппарат.
Опыт №1
Сахароза C 12 H 22 O 11 - дисахарид из группы олигосахаридов, состоящий из двух моносахаридов - α-глюкозы и β-фруктозы. . Сахароза является весьма распространённым в природе дисахаридом, она встречается во многих фруктах, плодах и ягодах. Особенно велико содержание сахарозы в сахарной свёкле и сахарном тростнике. Сахароза лучше растворяется в горячей воде.
Физические свойства: она представляет собой бесцветные кристаллы сладкого вкуса, хорошо растворима в воде, температура плавления сахарозы 160 °C, при застывании расплавленной сахарозы образуется аморфная прозрачная масса – карамель.
Химические свойства:
Сахароза имеет более сложное строение, чем глюкоза. Молекула сахарозы состоит из соединенных друг с другом остатков глюкозы и фруктозы. Наличие гидроксильных групп в молекуле сахарозы легко подтверждается реакцией с гидроксидами металлов. Если раствор сахарозы прилить к гидроксиду меди (II), образуется ярко-синий раствор сахарата меди. Альдегидной группы в сахарозе нет: при нагревании с аммиачным раствором оксида серебра (I) она не дает «серебряного зеркала», при нагревании с гидроксидом меди (II) не образует красного оксида меди (I) Сахароза является важнейшим из дисахаридов.Реакция сахарозы с водой.
При кипячении раствора сахарозы появляются молекулы с альдегидными группами, которые и восстанавливают гидроксид меди (II) до оксида меди (I). Эта реакция показывает, что сахароза при каталитическом действии кислоты подвергается гидролизу, в результате чего образуются глюкоза и фруктоза:
С 12 Н 22 О 11 + Н 2 О -> С 6 Н 12 O 6 + С 6 Н 12 O 6 .
Опыт №2
1. Физические свойства
Крахмал – это белый безвкусный порошок, нерастворимый в холодной воде и образующий коллоидный раствор (крахмальный клейстер) в горячей воде. Существует в двух формах: амилоза – линейный полимер, растворимый в горячей воде, амилопектин – разветвлённый полимер, не растворимый в воде, лишь набухает.
2. Нахождение в природе
Крахмал (C 6 H 10 O 5) n – основной источник резервной энергии в растительных клетках – образуется в растениях в процессе фотосинтеза и накапливается в клубнях, корнях, семенах
6CO 2 + 6H 2 O свет, хлорофилл → C 6 H 12 O 6 + 6O 2
nC 6 H 12 O 6 → (C 6 H 10 O 5) n + nH 2 O
глюкоза крахмал
Содержится в клубнях картофеля, зёрнах пшеницы, риса, кукурузы. Гликоген (животный крахмал), образуется в печени и мышцах животных.
Опыт №3
В холодной воде крахмал нерастворим, в горячей зерна его набухают и образуют густую жидкость - крахмальный клейстер.
Опыт №4
Это качественная реакция на крахмал. При взаимодействии йода с крахмалом образуется соединение включения (клатрат ) канального типа. Клатрат – это комплексное соединение, в котором частицы одного вещества внедряются в кристаллическую структуру «молекул-хозяев». В роли «молекул-хозяев» выступают молекулы амилозы, а «гостями» являются молекулы йода. Молекулы йода располагаются в канале спирали диаметром ~1 нм, создаваемой молекулой амилозы. Попадая в спираль, молекулы йода испытывают сильное влияние со стороны своего окружения (ОН-групп), в результате чего увеличивается длина связи I–I. Данный процесс сопровождается изменением бурой окраски йода на сине-фиолетовую.
Крахмал, как полисахарид, состоит из множества остатков глюкозы. Поэтому под действием растворов щелочей, кислот или ферментов крахмал подвергается гидролизу. Ступенчатый ферментативный гидролиз крахмала начинается еще в ротовой полости под воздействием ферментов слюны (амилазы и мальтазы).
Крахмал подвергается кислотному гидролизу, который протекает ступенчато и беспорядочно. При расщеплении он сначала превращается в полимеры с меньшей степенью полимеризации – декстрины , потом в дисахарид мальтозу, и в итоге – в глюкозу. Таким образом, получается целый набор сахаридов.
Или краткая форма записи уравнения:
Белки (протеины)
Белки – азотсодержащие биополимеры, состоящие из остатков аминокислот, связанных пептидной связью. В органике белки выполняют множество функций, включая структурную и ферментативную. Под действием различных факторов белки подвергаются денатурации. Белки – это незаменимая часть пищи. Основные источники полноценного белка – продукты животного происхождения.
Оборудование и реактивы: сырое куриное яйцо, клубень сырого и вареного картофеля, раствор перекиси водорода, разбавленный раствор йода, спички, ватные палочки, крахмальный клейстер, бинт, ножницы, столовый нож, пинцет, лист белой бумаги, пипетка, ложечка, стеклянные баночки, вода, электрочайник, фотоаппарат.
Опыт №1
При добавлении белка в воду не образуется однородный раствор. Растворы белков – коллоидные растворы.
К свойствам белковых растворов относятся:
1. Рассеивание света вследствие дифракции на коллоидных частицах – опалесценция . Особенно это заметно при прохождении луча света через белковый раствор, когда виден светящийся конус (эффект Тиндаля).
2. Белковые растворы в отличие от истинных обладают малой скоростью диффузии.
3. Неспособность белковых частиц проникать через мембраны, поры которых меньше диаметра белков (полунепроницаемые мембраны). Это используется в диализе . Очистка белковых препаратов от посторонних примесей лежит в основе работы "искусственной почки " при лечении острой почечной недостаточности.
4. Создание онкотического давления, то есть перемещение воды в сторону более высокой концентрации белка, что проявляется, например, как формирование отеков при повышении проницаемости сосудистой стенки.
5. Высокая вязкость в результате сил сцепления между крупными молекулами, что проявляется, например, при образовании гелей и студней.
Опыт №2
Под воздействием высокой температуры белок свернулся, в результате чего образовались хлопья. То есть произошла денатурация – разрушение вторичной и третичной структур белка с сохранением первичной структуры. Она происходит при нагревании, изменении кислотной среды, действии излучения. Могут разрушаться водородные, гидрофобные, дисульфидные и ионные связи. Денатурация бывает обратимой и необратимой. Необратимая денатурация может быть вызвана сильным нагреванием или образованием нерастворимых веществ.
В каждой живой клетке обмен веществ (метаболизм) происходит под действием ферментов. Ферменты – это биологические катализаторы белковой природы. Ферменты, которые катализируют разложение пероксида водорода Н2О2, называются каталазы или пероксидазы. В результате реакции образуется вода и молекулярный кислород.
Фермент каталаза, содержащийся в картофеле должен прореагировать с пероксидом водорода с образованием воды и молекулярного кислорода. В клетках сырого картофеля ферменты работоспособны, так как сохраняется структура белка. При варке картофеля произошла денатурация каталазы, в результате чего она утратила способность вступать в реакцию с перекисью водорода.
Опыт №4
|
Наблюдаю |
||
|
Бинт, крахмальный клейстер, раствор йода, ватную палочку, ножницы, вода. |
В клейстер опускаю на пару минут бинт длиной 30 см, вытаскиваю, просушиваю на листе белой бумаги. Когда бинт высох, разрезаю его на кусочки по 5 см. Кусочек этого бинта опускаю в стакан с раствором йода. Вытаскиваю бинт и раскладываю на листе белой бумаги. Смачиваю ватную палочку слюной и рисую букву на накрахмаленном кусочке бинта. Зажимаю кусочек между ладонями на некоторое время, после чего окунаю в раствор йода и высушиваю. Проделываю то же самое, что и в предыдущем случае, но ватную палочку смачиваю водой. |
Бинт полностью окрасился в синий цвет. После того, как бинт высох, на синем фоне четко видна написанная ранее буква. Бинт высох, но буква не проявилась. |
Когда мы опустили накрахмаленный бинт в раствор йода, то бинт окрасился в синий цвет. Окраску имеет комплекс иода с крахмалом, образование которого объясняют способностью молекул I2 помещаться в длинных полостях между витками спиралей, образованных молекулой крахмала. Полости заполнены плотно, и взаимодействия между молекулами достаточно сильны, чтобы обеспечить появление интенсивного окрашивания даже при очень низких концентрациях йода. Это качественная реакция на крахмал.
Воздействие слюны на крахмал называют ферментативным гидролизом. Так как сам крахмал является веществом инертным, то эта реакция происходит под воздействием тепла и катализатора. Им в нашем опыте является фермент слюны – амилаза. Именно он расщепляет крахмал на более мелкие составляющие, в частности, декстрины. Кусочек накрахмаленного бинта мы погрели в руках, чтоб активизировать работу ферментов. То место, куда была нанесена слюна, останется белым, а весь остальной участок окрасится в синий цвет. Это происходит потому, что слюна успела разложить крахмал на составные части, частично превратившись в глюкозу. Йод же не оказывает действия на глюкозу, поэтому написанная слюной буква не синеет.
В ином же опыте вместо слюны на бинт была нанесена вода, которая не разлагает крахмал на составные части. Следовательно, то место, куда была нанесена вода, останется синим.
Вывод: я углубила и закрепила знания об органических веществах, относящихся к классам белков (протеинов), жиров и углеводов; развила организационные, технические и интеллектуальные умения; воспитала интереса к химическому эксперименту и к самостоятельному получению знаний. Все эти вещества встречаются в нашей жизни повседневно. Они содержатся как продуктах (животного и растительного происхождения), так и в нашем организме. Эти органические соединения выполняют важные функции.
Жиры выполняют следующие функции:
1) Структурную (входят в состав клеточных мембран и нервной ткани);
2)Энергетическая (1 г. – 38,9 кДж);
3)Запасающая;
4)Защитная (защита организма от чужеродных микроорганизмов);
5)Гормональная (жиры вырабатывают цитокины, а также женские половые гормоны, входят в состав гормонов надпочечников);
6)Транспортная (жиры способствуют всасыванию микроэлементов, а также так называемых жирорастворимых витаминов (A,D,E и K);
7)Улучшают вкусовые качества пищи, тем самым вызывая активацию центра голода в продолговатом мозге.
8) Терморегуляторная (сохранение тепла в организме).
Функции углеводов:
1) Энергетическая (1г. – 17,6 кДж);
2) Запасающая (гликоген, крахмал);
3) Структурная (входит в состав ДНК, РНК, АТФ, образуют гликокаликс животной клетки);
4) Защитная (образуют вязкие секреты, слизи, стенки желез и компоненты слюны).
Функции белков:
1) Ферментативная (все химические реакции происходят при участии ферментов, которые ускоряют реакции в миллионы раз. Почти все ферменты по своей природе являются белками);
2) Транспортная (транспортные белки мембран обеспечивают постоянный состав клетки, а белок гемоглобин осуществляет перенос кислорода к органам и тканям);
3) Защитная (в ответ на проникновение различных чужеродных объектов в организме вырабатываются особые белки – антитела, которые обеззараживают антигены);
4) Регуляторная (многие гормоны – регуляторы роста и развития организма – белки. Белок инсулин регулирует содержание сахара в крови);
5) Двигательная (все движения обеспечиваются белками – актином и миозином, которые входят в состав мышечной ткани. В состав органов движения простейших входит белок тубулин);
6) Строительная (белки входят в состав клеточных мембран, рибосом и хромосом. Из белков состоят волосы, шерсть, ногти, чешуя. Эластин и коллаген придает коже упругость и эластичность);
7) Энергетическая (1г. – 17,6 кДж);
8) Питательная (белки – один из основных элементов питания человека и животного, при их недостатке в пище возникают тяжелые нарушения азотистого обмена)
Таким образом, белки, углеводы и жиры – являются источниками энергии для организма. Благодаря им может осуществляться метаболизм. Эти органические вещества выполняют все жизненно важные функции и являются источниками питания организма. Их недостаток ведет к развитию тяжелых нарушений здоровья.
Биоорганические соединения – углеводы, белки и липиды. 2
Углеводы. 2
Функции углеводов. 3
Строение моносахаридов. 6
Химические свойства моносахаридов. 8
Дисахариды. 9
Полисахариды. 10
Функции белков и пептидов. 13
Аминокислоты. 15
Аминокислоты, входящие в состав белков. 16
Получение аминокислот. 17
Химические свойства. 17
Липиды. 19
Функции липидов. 22
Физические свойства жиров. 24
Химические свойства жиров. 24
Описание задач практикума. 26
Тема углеводы. 26
1. Восстанавливающие свойства моно- и дисахаридов. 26
2. Ферментативный гидролиз крахмала. 26
3. Действие аммиачного раствора оксида серебра на глюкозу. 27
Данный опыт покажет вам одну из самых красивых реакций - реакцию серебряного зеркала. (так же качественная реакция). 27
5. Действие гидроксида меди(II) на глюкозу. 27
Данный эксперимент продемонстрирует реакцию медного зеркала. 27
Тема белки. 27
Цветные и качественные реакции на аминокислоты и белки. 27
Тема липиды. 27
Растворимость жиров. 27
Заключение. 28
Список литературы: 28
Введение.
Естественные науки, такие как биохимия, невозможно изучать без экспериментов. Поэтому в наше время очень актуально представлять учащимся не только теоретический материал, но и практический. Без сомнений, теоретический материал в учебных пособиях по биохимии представлен очень хорошо, однако практикум представлен очень скудно. Те эксперименты, которые включены в него, зачастую не получаются. Возможно, это связано с неточностями в описании экспериментов. Поэтому нужно составить такой практикум, где эксперименты давали бы положительные результаты.
Таким образом, Ццелью моей работы является составление практикума по биохимии.
В качестве практикума для анализа мной был выбран практикум по биологии
для 10 – 11 класса профильного уровня: Практикум для учащихся 10 – 11 классов по биологии «Профильный уровень» Г.М.Дымшиц, О.В. Саблина.
В процессе работы мной были поставлены следующие задачи:
1.Отобрать теоретический материал по определенным критериям.
Освоить программу по написанию химических формул ChemWindow
2. Написать текст, адаптированный для учащихся 10 класса теоретический материал.
Подобрать эксперименты.
3. Проделать опытыэксперименты и заснять их на камеру. – сделать видео, которое наглядно будет показывать учащимся порядок проведения опытов.
Сделать видео с помощью программы Windows Move Maker, которое наглядно будет показывать учащимся порядок проведения опытов.
Зачем делать видео к практикуму?
Для того, чтобы наглядно показать учащимся свойства определенного вещества,
Может служить пособием по проведению опыта.
В качестве контроля усвоения материала.
Отбор экспериментов проходил по следующим критериям: свойства органических веществ, качественные реакции, доступность реактивов и воспроизводимости экспериментов.
Биоорганические соединения – углеводы, белки и липиды.
Углеводы. 1
Углеводы – органические вещества с общей формулой С n (H 2 O) n , где n больше или равно 3, - служат источником энергии для животных и растительных клеток; во многих растениях они образуют также составные части клеток, клеточные оболочки и служат опорными элементами для всей клетки или растения. Растения обладают способностью синтезировать самые разнообразные углеводы из двуокиси углерода и воды в присутствии света. Углеводы являются основой для синтеза остальных органических веществ. В животных тканях число различных углеводов значительно меньше; к наиболее важным из этих относятся глюкоза, галактоза, гликоген и их полимеры.
реакция фотосинтеза.
Функции углеводов. 2
ФУНКЦИЯ | УРОВЕНЬ ОРГАНИЗАЦИИ | ПРИМЕРЫ |
Составная часть жизненно важных веществ клетки. | молекулярный | 1.Входит в состав носителей генетической информации – нуклеиновых кислот: рибоза – в состав РНК, дезоксирибоза – в состав ДНК. 2. Рибоза входит в состав основного носителя энергии клетки – АТФ. 3. Рибоза входит в состав акцепторов водорода – ФАД, НАД и НАДФ. |
Участие в фиксации углерода. | Клеточный | Пентоза рибулозодифосфат является непосредственным акцептором углекислого газа в темновой фазе фотосинтеза. |
Энергетическая. | Клеточный | Глюкоза является одним из наиболее распространенных дыхательных субстратов, т.е. источников получения энергии. |
Резервная | Организменный | 1. Крахмал является наиболее распространенным запасным веществом у растений. 2. Водорастворимые углеводы (сахароза, глюкоза, фруктоза) запасаются в клеточном соке растений. 3. У животных, прокариот и грибов. Резервным полисахаридом является гликоген. 4. Редуценты и симбиотическая микрофлора кишечника используют целлюлозу, так как они имеют специфические ферменты, гидролизирующие ее до глюкозы. |
Структурная. | Клеточный | 1. Целлюлоза составляет основную массу клеточных стенок бактерий и растительных клеток. 2. Хитин образует клеточные стенки грибов. |
Тканевый | 1. Углеводные компоненты гликокаликса обеспечивают узнавание клетками друг друга. Благодаря этому происходит ряд процессов: сперматозоиды опознают яйцеклетку своего биологического вида; клетки одного типа удерживаются вместе, образуя ткани; оттаргаются несовместимые органы при трансплантации. 2. Углеводные компоненты придают специфичность групповым веществам крови. 3. Гликокаликс микроворсинок кишечного эпителия является носителем ферментов пристеночного пищеварения. 4. Гепарин (производное полисахаридов препядствует свертыванию крови). |
|
Организменный | 1. Хитин образует покровы тела членистоногих. 2. Муреин образует опору клеточной стенки бактерий – клеточный мешок. |
|
Защитная | Тканевый | 1. Углеводные компоненты гликокаликса являются рецепторами тканевой совместимости, а также выполняют рецепторную функцию при фагоцитозе. 2. Вязкие растворы полисахаридов выстилают полости дыхательного и пищеварительного трактов и защищают от механических повреждений ткани и органы. |
Организменный | 1. Камеди (производные моносахаридов), выделяющиеся в местах повреждения стволов и ветвей, защищают деревья и кустарники от проникновения инфекции через раны. 2. Слизи (полисахариды) разбухают во влажной среде и тем самым защищают от пересыхания зародыши прорастающих семян. 3. Твердые клеточные стенки одноклеточных организмов или хитиновый покров членистоногих защищают от неблагоприятных воздействий внешней среды. |
Строение и свойства углеводов .

Можно схему!Углеводы, имеющие биологическое значение, делятся на три класса: моносахариды, дисахариды и полисахариды. Моно- и дисахариды, обычно называемые сахарами, легко растворимы в воде, могут кристаллизироваться и легко проходят через мембраны. В отличие от них полисахариды не кристаллизируются и не проходят через мембраны.
Моносахариды – такие углеводы, которые не могутгидролизоваться с образованием более простых углеводов
Моносахариды представляют собой простые сахара с формулой С n (H 2 O) m . В зависимости от числа углеродных атомов в их молекуле различают триозы, пентозы, гексозы, гептозы. В природе наиболее распространены пентозы (рибоза и дезоксирибоза) и гексозы (глюкоза, фруктоза).
Все моносахариды разделяют на альдозы и кетозы в зависимости от того, имеются ли в молекуле моносахарида альдегидная или кетонная группа. Простейший моносахарид – глицериновый альдегид (С3H6O3):

глицериновый альдегид .
Остальные моносахариды делят на группы по числу атомов кислорода (обычно это число равно числу атомов углерода): тетрозы (С4H8O4), пентозы (С 5 H 10 O 5) и гексозы (С 6 H 12 O 6).
Строение моносахаридов .
Глюкоза и фруктоза являются изомерами – их строение различно, но молекулярные формулы совпадают – С 6 H 12 O 6 .
![]()

Глюкоза Фруктоза

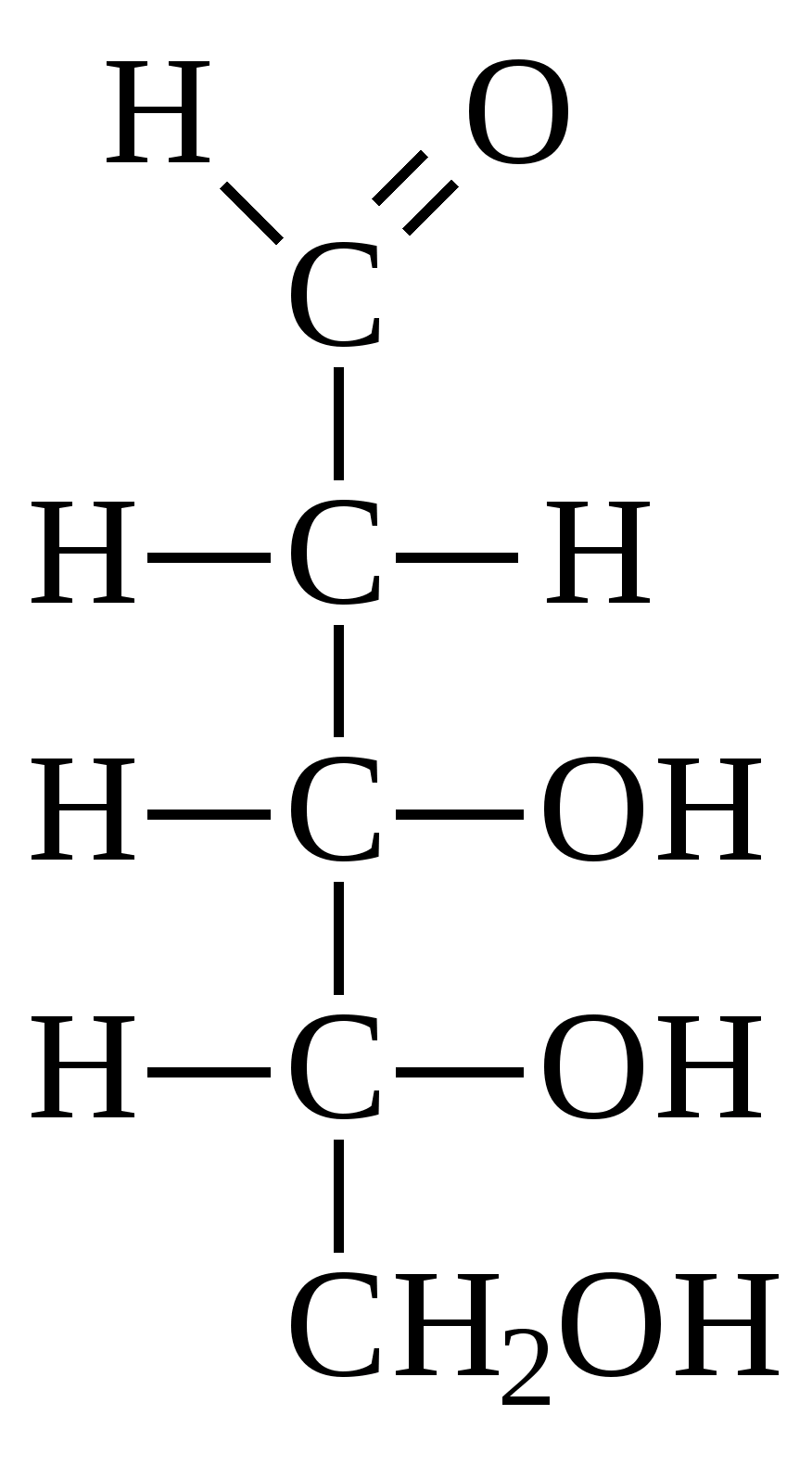
Рибоза Дезоксирибоза
Сахара могут также существовать и в виде циклов. Сахара с шестичленными циклами называю пиранозными , а сахара с пятичленным циклом называют фуранозными.
 Фуранозный цикл
Фуранозный цикл  Пиранозный цикл.
Пиранозный цикл.
 β – Глюкоза.
β – Глюкоза. 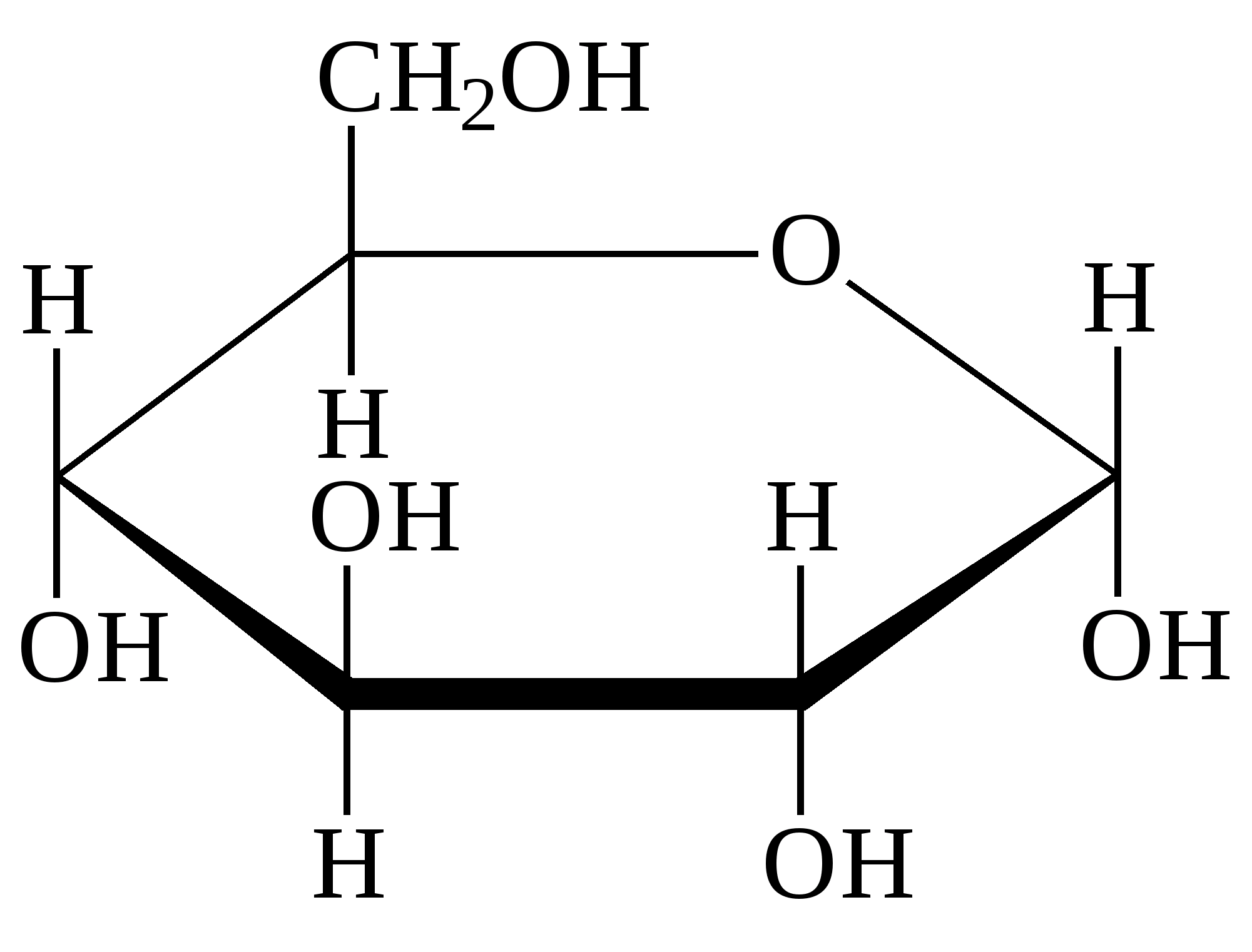 α – Глюкоза.
α – Глюкоза.
 Рибоза.
Рибоза.  Дезоксирибоза.
Дезоксирибоза.
Названия моносахаридов содержат греческие названия числа атомов кислорода (углерода) и окончание –оза (тетроза, пентоза, гексоза).
Наличие альдегидной группы обозначают прибавлением приставки альдо- (глюкоза – альдогексоза), наличие кетонной группы выражается наличием приставки кето – (фруктоза – кетогексоза).
Изомерия моносахаридов обусловлена наличием:
Альдегидной или кетонной группы (структурная изомерия)
Асимметричностью атома углерода(одного или нескольких), следовательно, оптическая изомерия.
Пространственная изомерия.
Количество изомеров у сахаров очень велико.
Моносахариды выделяют из природных объектов. Глюкозу чаще всего получают гидролизом крахмала в присутствии серной кислоты.
nC 6 H 12 O 6 → (C 6 H 10 O 5) n + nH 2 O
Кроме того многие моносахарид встречаются в природе в свободном виде, например мед – смесь фруктозы и глюкозы.
Химические свойства моносахаридов.
Химические свойства моносахаридов определяются наличием в их молекулах гидроксильных групп и карбонильной группы.
Реакции альдегидной группы :
Восстановление альдегидной группы приводит к образованию шестиатомного спирта (сорбита):
Окисление мягкими окислителями (хлорная или бромная вода) приводит к образованию одноосновной кислоты (окисляется только альдегидная группа). Сильные окислители превращают в СOOH группу не только альдегидную, но и первичную спиртовую группу с образованием двухосновной кислоты.
Как и все альдегиды, глюкоза вступает в реакцию серебряного зеркала.
НОСН 2 (СНОН) 4 СHO + 2 OH => НОСН 2 (CHОН) 4 СООH + 2 Ag + 3NH 3 + H 2 O
Реакции гидроксильных групп .
1). Глюкоза может образовывать сложные эфиры – ациклирование глюкозы.
2). Качественные реакции с гидроксидом меди (II).
Реакции брожения.
Брожением называют процесс, при котором происходит расщипление моносахаридов некоторыми микроорганизмами. В зависимости от основных продуктов, получающихся при брожении, различают следующие виды брожения:
Спиртовое:
Молочнокислое:
Маслянокислое:
Дисахариды.
Олигосахариды – продукты конденсации нескольких (от 2 до 8, чаще всего – двух) молекул моносахаридов.
Дисахариды – это олигосахариды, молекулы которых состоят из двух циклических моносахаридных остатков (одинаковых или разных).
В зависимости от того, участвуют ли в создании связи между остатками моносахаридов два гликозидных гидроксила обоих моносахаридов, или один гидроксильный гликозил, различают две группы дисахаридов, отношение к окислителям которых различно: невосстанавливающиеся и восстанавливающиеся.
Примером сахарида первого типа является сахароза. Она не дает качественных реакций на альдегидную группу и способна вступать только в реакции характерные для гидроксильных групп.
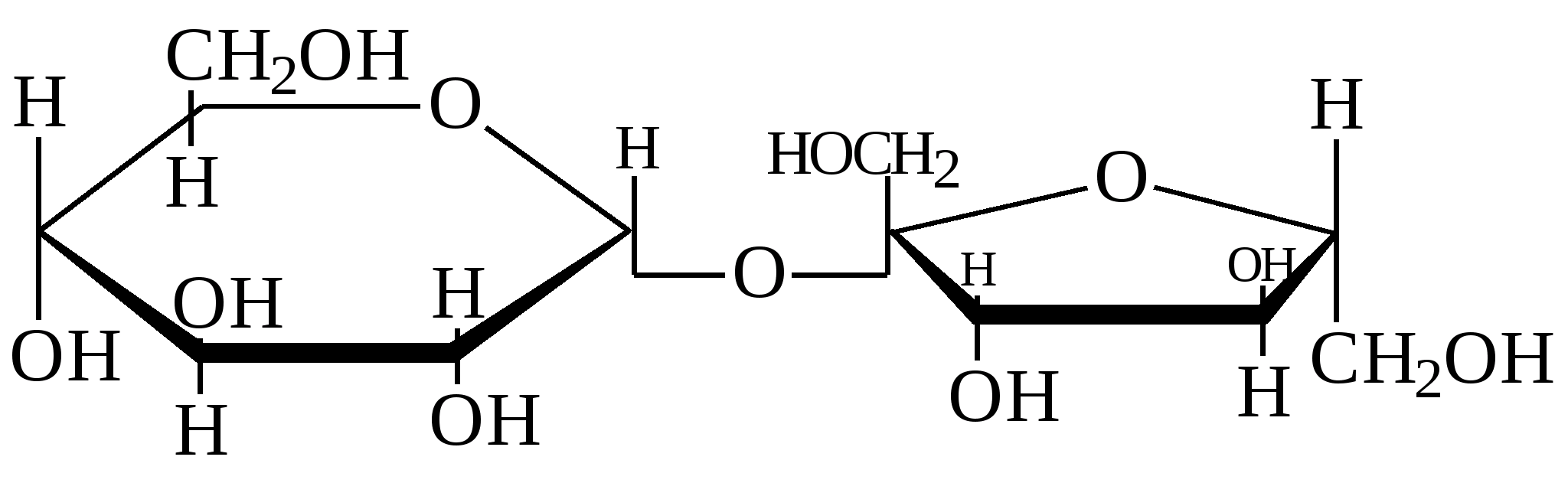
сахароза
Пример сахарида второго типа – лактоза. В растворе молекулы этого типа могут переходить из циклической в альдегидную форму; отсюда и их восстановительные свойства: они дают реакцию «серебряного зеркала» и способны окисляться до монокарбоновых кислот.
Все дисахариды способны превращаться при гидролизе в моносахариды.
Сахароза глюкоза фруктоза
Дисахариды получают из природных источников, таких как сахарная свекла или сахарный тростник (получают сахарозу). Лактоза (молочный сахар) содержится в молоке.

Мальтоза.

Лактоза.
Полисахариды.
Полисахариды образуются путем соединения многих моносахаридов и имеют формулу (С 6 Н 10 О 5) n . При гидролизе они дают молекулы простых сахаров. Набольшее биологическое значение имеют полисахариды крахмал и гликоген, являющиеся резервными веществами в клетках растений и животных соответственно, и целлюлоза –важнейший структурный элемент растительной клетки. Целлюлоза состоит из нескольких сотен молекул глюкозы. С увеличением числа мономеров растворимость сахаридов падает.
Крахмал – это природный полисахарид образованный остатками глюкозы. Крахмал образуется в растениях при фотосинтезе. Наиважнейшим из свойств крахмала является его гидролиз, конечным продуктом которого является глюкоза.
Крахмал не является индивидуальным веществом – это смесь полисахаридов амилопектина и амилозы, которые состоят из остатков глюкозы, соединенных гликозидными связями.
 Крахмал.
Крахмал.
Крахмал является основным источником углеводов в пище человека: в больших количествах крахмал содержится в хлебе, крупах и овощах.
Наиболее важным химическим свойством крахмала является его гидролиз, конечным продуктом которого является глюкоза.
Целлюлоза (клетчатка) – наиболее распространенный в растительном мире полисахарид. Из целлюлозы состоят клетки стенок растений. Молекулы целлюлозы в отличие от крахмала имеют только линейное строение, причем цепи расположены параллельно друг другу и соединены между собой множеством водородных связей – отсюда неспособность целлюлозы растворяться в воде.
 n
n
Целлюлоза
Молекула целлюлозы состоит из остатков βb – глюкозы, связанных через первый и четвертичный атом углерода.
Целлюлоза способна образовывать сложные эфиры.
Гидролиз целлюлозы приводит к образованию глюкозы.
Сбраживание глюкозы приводит к образованию этилового спирта, который в этом случае называют гидролизным.
Хитин. По своей структуре и функции хитин очень близок к целлюлозе, это тоже структурный полисахарид. Хитин встречается у некоторых грибов, где он играет в клеточных стенках опорную роль благодаря своей волокнистой структуре, а также у некоторых групп животных (членистоногих) в качестве важного компонента их наружного скелета.
Гликоген – резервный полисахарид, основной запасной углевод у животных и человека. Он постоянно синтезируется организмом и накапливается во всех его тканях. Структура гликогена очень близка к структуре амилопектина – компонента крахмала. Оба из остатков состоят из остатков β a – глюкозы, соединенных между собой гликозидными связями двух типов: С(1) – О – (С)4 и (С)1 – O – (C)6. Гликоген отличается от амилопектина прежде всего своей молекулярной массой. Молекула гликогена отличается более плотной, компактной и глобулярной структурой.
Белки. 3
Белки – обязательная составная часть всех клеток. В жизни органических соединений белки имеют первостепенное значение. В состав белка входят углерод, азот, водород, некоторые белки содержат еще и серу. Роль мономеров в белках играют аминокислоты. У каждой аминокислоты имеется карбоксильная группа (-COOH) и аминогруппа (-NH 2). Наличие в одной молекуле кислотной и основной группы обуславливает их высокую реактивность. Между соединившимися кислотами возникает связь….., называемая пептидной, а образовавшееся соединение из нескольких аминокислот называется пептидом. Соединение из большого числа аминокислот называется полипептидом. В белках встречаетсяНаиболее распространены 20 аминокислот, отличающихся своим строением. Разные белки образуются в результате соединения аминокислот в разной последовательности. Огромное разнообразие живых существ в значительной степени определяется различиями в составе имеющихся у них белков.
В строении молекул белков различают 4 уровня организации.
Первичная структура – полипептидная цепь из аминокислот, связанных в определенной последовательности ковалентными пептидными связями.
Например, молекула инсулина состоит из 2- полимерных цепочек; одна цепочка состоит из 21 остатка, а вторая 30
Вторичная структура – полипептидная цепь, закрученная в виде спирали. В ней между соседними витками возникают мало прочные водородные связи. В комплексе они обеспечивают довольно прочную структуру.
Третичная структура представляет собой причудливую, но для каждого белка специфическую конфигурацию – глобулу. Она удерживается мало прочными гидрофобными связями или силами сцепления между полярными радикалами, которые встречаются у многих аминокислот. Благодаря их многочисленности они обеспечивают достаточную устойчивость белковой макромолекулы и ее подвижность. Третичная структура белков поддерживается также ковалентными S-S связями, возникающими между удаленными друг от друга радикалами серосодержащей аминокислоты – цистеина.
Благодаря соединению нескольких молекул белков между собой образуется четвертичная структура. Если пептидные цепи уложены виде клубка, то такие белки называются глобулярными. Если пептидные цепи уложены в пучки нитей, они носят название фибриллярных белков.
Нарушение природной структуры белка называют денатурацией. Она может возникать под действием температуры, химических веществ, радиации и т.д. Денатурация может быть как обратимой, так и необратимой.
Функции белков и пептидов. 4
Функции. | Уровень организации . | Примеры. |
Структурная. | Доклеточный. | Составляет капсиды вирусов. |
Клеточный. | Обязательный компонент всех мембран клетки |
|
Тканевый и органный. | Коллаген – компонент соединительной ткани и кожи. Кератин – компонент перьев, шерсти, волос, рогов, копыт, ногтей, когтей |
|
Организменный. | Склеротин входит в состав покровов тела насекомых. |
|
Транспортная. | Клеточный. | Участие в активном транспорте веществ через клеточные мембраны против градиента концентраций. Диффузия через клеточный мембраны. |
Организменный. | Гемоглобин переносит кислород и углекислый газ в крови позвоночных. Сывороточный альбумин переносит жирные кислоты. Различные глобулины переносят ионы металлов и гормонов. |
|
Двигательная. | Клеточный. | Тубулины микротрубочек обеспечивают работу веретена деления клеток. Флагеллин обеспечивает движение жгутиков прокариот. |
Организменный. | Актин и миозин обеспечивают сокращение волокон поперечнополосатой мускулатуры, за счет чего совершается передвижение тела животных и человека |
|
Рецепторная. | Тканевый. | Гликопротеины являются компонентами гликокаликса. Гликопротеины – антигены тканевой совместимости – ответственны за распознавание тканей. |
Организменный. | Опсин – составная часть светочувствительных пигментов родопсина и йодопсина, находящихся в клетке сетчатки глаза. |
|
Защитная. | Клеточный. | Антитела связывают инородные белки, образуя с ними комплексы. Интерфероны – универсальные противовирусные белки |
Тканевый. | Тромбопластин, протромбин, тромбин и фибриноген предохраняют организм от кровопотери, образуя тромб. Антиоксидантные ферменты (каталаза), препятствует развитию свободно радикальных процессов, очень важных для организма |
|
Организменный. | Кожа, в формировании которой принимают участие различные белки, защищает тело позвоночных. |
|
Ферментативная. | Клеточный. | Большинство ферментов является белками. |
Организменный. | Белки – основной источник аминокислот. Казеин молока- источник белка для детенышей млекопитающих и человека. |
|
Запасающая. | Органный. | Ферритин – запасает железо в печени, селезенке, яичном желтке. |
Организменный. | Альбумин – запасает воду в яичном желтке. Белки семян растений семейства бобовых – источник питания для зародыша. |
|
Регуляторная. | Организменный. | Нейропептиды – пептиды, присутствующие в мозге и влияющие на функции ЦНС. | Руководство
Правильное питание помогает откорректировать вес, увеличить пользу от физических нагрузок, и конечно же, укрепить здоровье. Вся пища, которую мы употребляем, тщательно формирует наш организм. Несколько важных советов об особенностях белков, жиров и углеводов помогут устранить множество ошибок при составлении ежедневного рациона.
Правильные белки
Человеческий организм в большей степени состоит из белка, поскольку именно белок выполняет строительную функцию, влияющую на гормональный фон и выработку необходимых ферментов. В состав белка входят различные аминокислоты, многие из которых крайне важны для нормализации обмена веществ. При этом все белки делятся на животные и растительные.
Животные белки
К животным белкам прежде всего относят:
- мясо;
- рыба;
- молоко;
- яйца.
Особенности:
- Данные продукты содержат максимум полезных аминокислот и имеют высокую концентрацию белка.
- Чрезмерное употребление высококонцентрированных белком продуктов увеличивает нагрузку на печень, поджелудочную железу и почки.
- Присутствие вредных веществ, таких как антибиотик, холестерин.
Растительные белки
К растительным белкам относят:
- бобовые (фасоль, чечевица)
- орехи
- семена
- сыр тофу
- соевое молоко.
Особенности:
- Правильное сочетание зерновых и бобовых дают полное насыщение аминокислотами.
- Растительные продукты вместо вредных компонентов содержат полезные углеводы.
- Соевый состав наполнен фитоэстрогенами.
- Концентрация белков значительно ниже.

Правильные жиры
Жиры — это жизненная сила, полученная организмом за счет впитывания специальных жирных аминокислот. Также они играют весомую роль при усвоении витаминов. Однако растительные и животные жиры имеют разные свойства.
Растительные жиры
- растительные масла;
- орехи;
- авокадо;
- оливки.
Особенности:
- Выведение холестерина, предупреждение атеросклероза.
- Лёгкое усвоение за счет незначительной концентрации жиров.
- Улучшение работы кишечника.
- Поддержание оптимальной жировой среды кожного покрова.
- Пользу несут только необработанные растительные жиры.

Животные жиры
- мясные изделия;
- рыба;
- молочные и кисло-молочные продукты;
- маргарин;
- яйца.
Особенности:
- Жиры молочных продуктов быстрее выводятся из организма.
- Животные жиры перегружают организм из-за низкого содержания аминокислот.
- Количество животных жиров должно быть в два раза меньше растительных.

Незаменимые жиры
В особую категорию попадают жиры, полезная ценность которых предельно высока, но они не могут самостоятельно вырабатываться организмом. Поэтому ими обогащать организм возможно только при помощи пищи. Содержание незаменимых жиров (Омега 3) присутствует в следующих продуктах:
- масло зародышей пшеницы,
- масло грецкого ореха,
- масло льняного семени,
- рыбий жир.

Правильные углеводы
Для должного функционирования белков и жиров непременно требуются углеводы. В организме они же являются главным «энергетиком». Углеводы делятся на простые и сложные, и входят в состав таких продуктов:
- фрукты и овощи,
- хлебные изделия,
- крупы,
- макароны,
- картофель.
Специалисты рекомендуют чаще употреблять сложные углеводы, так как они богаты витаминами и всеми необходимыми микроэлементами для очищения организма от токсинов. Они выступают в форме инсулина, целлюлозы, гликогена и крахмала, а содержатся в листьях салата, топинамбуре, огурцах, капусте, макаронных изделиях, муке и хлебе.

Помните, правильные углеводы должны составлять как минимум половину ежедневного рациона. Меньше всего следует употреблять жиры, однако полностью исключать их из рациона неэффективно. Поэтому разделите их с белками в пользу последних. Будьте здоровы!
Введение. 2
I. Общая характеристика, свойства, функции белков. 3-5
II. Общая характеристика, свойства, функции углеводов. 5-7
III. Общая характеристика, свойства, применение жиров. 8-12
IV. Минеральные вещества. 12-18
Заключение. 19
Список литературы. 20
Введение.
Мы знаем, что наша пища состоит из белков, жиров, углеводов, минеральных веществ, воды, а также содержит витамины. Сегодня созданы пищевые консерванты, ароматизаторы и красители. В связи с этим появился новый раздел химии – химия пищи. Данный раздел появился относительно недавно, так как нужно было исследование продуктов питания созданных генной инженерией, изучение веществ, созданных для улучшения вкуса, цвета и хранения продукта. В данном реферате я расскажу об основных составляющих пищи, т.е. об основах химии пищи – белках, жирах, углеводах, минеральных веществах, об их важности и о сложном химическом составе.
I. Общая характеристика, свойства, функции белков.
I.I. Общая характеристика
Белки - это азотсодержащие высокомолекулярные органические вещества со сложным составом и строением молекул. Белок можно рассматривать как сложный полимер аминокислот. Белки входят в состав всех живых организмов, но особо важную роль они играют в животных организмах, которые состоят из тех или иных форм белков (мышцы, покровные ткани, внутренние органы, хрящи, кровь).Растения синтезируют белки (и их составные части -аминокислоты) из углекислого газа СО2 и воды Н2О за счет фотосинтеза, усваивая остальные элементы белков (азот N, фосфор Р, серу S, железо Fe, магний Mg) из растворимых солей, находящихся в почве. Животные организмы в основном получают готовые аминокислоты с пищей и на их базе строят белки своей организма. Ряд аминокислот (заменимые аминокислоты) могут синтезироваться непосредственно животными организмами. Характерной особенностью белков является их многообразие, связанное с количеством, свойствами и способах соединения входящих в их молекулу аминокислот. Белки выполняют функцию биокатализаторов ферментов, регулирующих скорость и направление химических реакций в организме. В комплексе с нуклеиновыми кислотами обеспечивают функции роста и передачи наследственных признаков, являются структурной основой мышц и осуществляют мышечное сокращение. В молекулах белков содержатся повторяющиеся амидные связи С(0)NH, названные пептидными (теория русского биохимика А.Я.Данилевского). Таким образом, белок представляет собой полипептид, содержащий сотни или тысячи аминокислотных звеньев.
Структура белков.
Особый характер белка каждого вида связан не только с длиной, составом и строением входящих в его молекулу полипептидных цепей, но и с тем, как эти цепи ориентируются. В структуре любого белка существует несколько степеней организации:
1.Первичная структура белка специфическая последовательность аминокислот в полипептидной цепи.
2.Вторичная структура белка способ скручивания полипептидной цепи в пространстве (за счет водородной связи между водородом амидной группы NH и карбонильной группы СО, которые разделены четырьмя аминокислотными фрагментами).
3. Третичная структура белка реальная трехмерная конфигурация закрученной спирали полипептидной цепи в пространстве (спираль, скрученная в спираль). Третичная структура белка обуславливает специфическую биологическую активность белковой молекулы. Третичная структура белка поддерживается за счет взаимодействия различных функциональных групп полипептидной цепи: дисульфидный мостик (-S-S-) между атомами серы, сложноэфирный мостик между карбоксильной группой (-СО-) и гидроксильной(-ОН), солевой мостик - между карбоксильной (-СО-) и аминогруппами (NH2).
4. Четвертичная структура белка тип взаимодействия между несколькими полипептидными цепями. Например, гемоглобин представляет из себя комплекс из четырех макромолекул белка.
I . II
Физические свойства.
Белки имеют большую молекулярную массу (104107 г/моль), многие белки растворимы в воде, но образуют, как правило, коллоидные растворы, из которых выпадают при увеличении концентрации неорганических солей, добавлении солей тяжелых металлов, органических растворителей или при нагревании (денатурация).
Химические свойства.
1. Денатурация разрушение вторичной и третичной структуры белка.
2. Качественные реакции на белок: биуретовая реакция: фиолетовое окрашивание при обработке солями меди в щелочной среде (дают все белки), ксантопротеиновая реакция: желтое окрашивание при действии концентрированной азотной кислоты, переходящее в оранжевое под действием аммиака (дают не все белки), выпадение черного осадка (содержащего серу) при добавлении ацетата свинца (II), гидроксида натрия и нагревании. 3. Гидролиз белков при нагревании в щелочном или кислом растворе с образованием аминокислот.
I . III . Биологические функции белков.
Множество химических связей, характерных для белковых макромолекул, предопределяет их функциональное многообразие.
1. Каталитические – относятся к биологическим катализаторам.
2. Транспортные – выполняет функции переноса веществ из одного компартмента клетки в другую или между органами целого организма.
3. Регуляторные – регуляторные функции, в первую очередь к ним относятся гормоны.
4. Защитные – представлены антителами или иммуноглобулинами.
5. Сократительные – позволяют сокращаться и перемещаться, обычно содержатся в мышечной ткани.
6. Структурные – входят в состав мембран клеток.
7. Рецепторные – участвуют при передаче нервного или гормонального сигнала.
8. Запасные и питательные – резервный и питательный материал клетки.
9. Токсические – представлены токсинами яда змей, скорпионов, пчел.
Наибольше всего мы употребляем запасные и питательные белки (например, мясо, питательный белок птичьих яиц, молоко и другие).
Наиболее часто употребляемые человеком белки:
Альбумины – белки животных и растительных тканей. Они относятся к питательным белкам. Отличия Альбуминов в животной клетке и растительной заключается в разном количестве метионина и триптофана. А также множество сложных белков липопротеины, гликопротеины, фосфопротеины, хромопротеины.
Фрагмент молекулы хромопротеина.
Продукты с наибольшим содержанием белка (на 100г продукта): кисломолочные продукты (творог, сыр), яйца куриные ( I категории), свинина, рыба, икра осетровая, орехи фундук.
II . Общая характеристика, свойства, функции углеводов.
II . I . Общая характеристика.
Углеводы – важный класс природных веществ – встречаются повсеместно в растительных, животных и бактериальных организмах.
Углеводы – это не очень удачный термин, поскольку так называют большое количество соединений, обладающих различной химической структурой и биологическими функциями. Более 100 лет назад этим термином было предложено называть природные соединения, состав которых соответствовал формуле (CH 2 O) n , т.е. гидраты углерода. По мере открытия новых углеводов оказалось, что не все они соответствуют этой формуле, а некоторые представители других классов обладают такой же формулой. Большой вклад в развитие учения об углеводах внесли отечественные ученые А.М. Бутлеров, А.А. Колли, Н.Н. Кочетков.
Углеводы включают соединения, начиная от низкомолекулярных, содержащих всего несколько атомов углерода, до веществ, молекулярная масса которых достигает нескольких миллионов.
Углеводы составляют 80% массы сухого вещества растений и около 2% сухого вещества животных организмов.Животные и человек не способны синтезировать сахара и получают их с различными пищевыми продуктами растительного происхождения.
Углеводы
![]()
![]()
Простые Сложные
МОНОСАХАРИДЫ ДИСАХАРИДЫ
Тетрозы С 4 Н 8 О 4 сахароза C12H22O11
элитроза лактоза
треоза мальтоза
Пентозы С 5 Н 10 О 5 целобиоза
арабиноза ПОЛИСАХАРИДЫ
ксилоза (С 5 Н 8 О 4) n
рибоза пентозаны
ГЕКСОЗЫ С 6 Н 12 О 6 (С 6 Н 10 О 5) n
глюкоза целлюлоза
манноза крахмал
галактоза гликоген
фруктоза


Дисахариды
Сахароза Трегалоза
II . II . Физические и химические свойства.
Физические свойства.
Моносахариды - это твердые вещества, способные кристаллизоваться. Они гидроскопичны, очень легко растворимы в воде, легко образуют сиропы, из которых выделить их в кристаллическом виде бывает очень трудно.
Дисахариды - кристаллические углеводы, молекулы которых построены из соединённых между собой остатков двух молекул моносахаридов.
Молекулы полисахаридов можно рассматривать как продукт поликонденсации моносахаридов. Общая формула полисахаридов (СбН10О5)п. Мы рассмотрим важнейшие природные полисахариды - крахмал и целлюлозу.
Химические свойства.
1. Свойства,характерные для спиртов:
Взаимдействие с карбоновыми кислотами с образованием сложных эфиров (реакция этерификации).
2. Свойства, характерные для альдегидов: взаимодействие с оксидом серебра (I) в аммиачном растворе (реакция "серебряного зеркала").
3. Специфические реакции - брожение: спиртовое брожение.
4. Сахароза подвергается гидролизу - разложению в присутствии минеральной кислоты и повышенной температуре на глюкозу и фруктозу.
С12Н22О11 + Н2О = С6Н12О6 +С6Н12О6
сахароза фруктоза глюкоза
II . III Биологические функции.
Для большинства организмов природные углеводы выполняют две основные функции: являются источниками углерода, который необходим для синтеза белков, нуклеиновых кислот, липидов и другие, обеспечивает до 70% потребности организма в энергии. При окислении 1г углеводов выделяется 16,9 кДж энергии.
Другими функциями углеводов являются следующие:
1. Резервная. Крахмал и гликоген представляют собой форму хранения питательных веществ.
2. Структурная. Целлюлоза и многие полисахариды входят в состав мембран растительных клеток
3. Защитная. Кислые гетерополисахариды выполняют роль смазочного материала, выстилая трущиеся поверхности суставов, дыхательных и пищеварительных путей.
4. Участие в создании комплексных молекул, например, гликопротеины.
Продукты с наибольшим содержанием углеводов (на 100г продукта): сахар-рафинад, крупы, хлебобулочные изделия, макаронные изделия.
III . Общая характеристика, свойства, применение жиров.
III . I . Общая характеристика. Физические и химические свойства.
Жиры, органические соединения, полные сложные эфиры глицерина (триглицериды) и одноосновных жирных кислот; входят в класс липидов. Наряду с углеводами и белками Ж. - один из главных компонентов клеток животных, растений и микроорганизмов. Строение Ж. отвечает общей формуле:
CH-О-CO-R’’
CH2-O-CO-R’’’,
где R’, R’’ и R’’’ - радикалы жирных кислот. Все известные природные жиры содержат в своём составе три различных кислотных радикала, имеющих неразветвлённую структуру и, как правило, чётное число атомов углерода. Из насыщенных жирных кислот в молекуле жиры чаще всего встречаются стеариновая и пальмитиновая кислоты, ненасыщенные жирные кислоты представлены в основном олеиновой, линолевой и линоленовой кислотами.
Жиры нерастворимы в воде, хорошо растворимы в органических
растворителях, но обычно плохо растворимы в спирте. При обработке перегретым паром, минеральными кислотами или щёлочью жиры подвергаются гидролизу (омылению) с образованием глицерина и жирных кислот или их солей образуя мыла. При сильном взбалтывании с водой образуют эмульсии. Примером стойкой эмульсии жиров в воде является молоко. Эмульгирование жиров в кишечнике (необходимое условие их всасывания) осуществляется солями жёлчных кислот.
Природные жиры подразделяют на жиры животные и растительные
(масла жирные). В организме жиры - основной источник энергии. Энергетическая ценность жиров в 2 с лишним раза выше, чем углеводов. Жиры, входящие в состав большинства мембранных образований клетки и субклеточных органелл, выполняют важные структурные функции. Благодаря крайне низкой теплопроводности жиров, откладываемый в подкожной жировой клетчатке, служит термоизолятором, предохраняющим организм от потери тепла, что особенно важно для морских теплокровных животных (китов, тюленей и др.). Вместе с тем жировые отложения обеспечивают известную эластичность кожи. Содержание жира в организме человека и животных сильно варьирует. В некоторых случаях (при сильном ожирении, а также у зимнеспящих животных перед залеганием в спячку)
запасные (откладываются в подкожной жировой клетчатке и в сальниках) и
протоплазматические (входят в состав протоплазмы в виде комплексов с
белками, называемые липопротеидами). При голодании, а также при
недостаточном питании в организме исчезает запасной жир, процентное же
содержание в тканях протоплазматических жиров остаётся почти без изменений даже в случаях крайнего истощения организма. Запасный жир легко извлекается из жировой ткани органическими растворителями. Протоплазматические жиры удаётся извлечь органическими растворителями только после предварительной обработки тканей, приводящей к денатурации белков и распаду их комплексов с жирами.
В растениях жиры содержатся в сравнительно небольших количествах.
Исключение составляют масличные растения, семена которых отличаются высоким содержанием жира.
Жиры в живых организмах в присутствии ферментов гидролизуются. Кроме рефкции с водой, жиры взаимодействуют также со щелочами:

Так как в состав растительных масел входят сложные эфиры непредельных карбоновых кислот, то их можно подвергнуть гидрированию:

III . II . Применение жиров.
Жиры в основном применяются в качестве пищевого продукта. К группе пищевых жиров относятся следующие виды жиросодержащей продукции: растительные масла, маргарин, майонез, кулинарные жиры, животные жиры. Свойства и пищевая ценность жиров зависят от соотношения в их составе насыщенных и ненасыщенных жиров. Жиры, в которых преобладают ненасыщенные жирные кислоты имеют твердую консистенцию, высокую температуру плавления, низкую усвояемость. В жидких растительных маслах преобладают ненасыщенные эфирные кислоты.
Ненасыщенные жирные кислоты влияют на количество холестерина, стимулируют его окисление и выведение из организма, повышают эластичность кровеносных сосудов, активизируют ферменты желудочно-кишечного тракта, повышают устойчивость к инфекционным заболеваниям и действию радиации.
Пищевые жиры используют непосредственно в пищу, для приготовления консервов, кондитерских и других изделий.
В процессе хранения жиры окисляются и приобретают неприятный вкус и запах. Окисляются жиры быстрее при повышенных температурах и на свету. Особенно быстро прогоркают жиры, содержащие много ненасыщенных жирных кислот (рыбий жир, куриный жир).
Растительные масла
Состояние рынка растительных масел
Подумать только: еще несколько лет назад у российского покупателя не было проблем с выбором растительного масла. На прилавках встречались только подсолнечное, кукурузное и иногда оливковое. А теперь, когда глаза разбегаются от предлагаемых названий и производителей, потребителю и товароведам-экспертам необходимы основополагающие знания, чтобы разобраться в этом многообразии.
На рынке растительного масла, пользующегося у российского потребителя неизменным успехом, поскольку его добавляют и в салаты, и широко используют при жарении, покупателю иногда трудно выбрать качественное масло из широко рекламируемого низкокачественного.
Поэтому как у производителя, так и у реализатора возникают соблазны подделать или увеличить объемы своей реализации путем подмены одного вида масла другим, менее ценным. Кроме того, на сегодняшний день на рынок поступает не только пищевое масло, но и масло техническое, технологически переработанное под пищевое. Поэтому возникают проблемы с проведением всесторонней экспертизы подлинности всех видов растительных масел, реализуемых на продовольственных рынках России.
При проведении экспертизы подлинности растительных масел могут достигаться следующие цели исследования: идентификация вида растительного масла; идентификация сорта растительного масла;
способы фальсификации и методы их выявления.
При проведении экспертизы подлинности с целью идентификации вида растительного масла эксперт должен владеть современными методами исследования данной группы товаров, а затем уже определить для себя круг решаемых им при этом задач исходя из своего уровня знаний в этой области.
Идентификация растительных масел.
Растительное масло - это готовый к употреблению продукт, полученный из семян или зародышей семян, плодов растений путем прессования и/или экстракции и очищенный от тех или иных примесей в зависимости от вида получаемого изделия.
По виду жиросодержащего сырья растительное масло вырабатывается: подсолнечное, кукурузное, горчичное, хлопковое, соевое, арахисовое, оливковое, кунжутное (сезамовое), кокосовое, пальмоядровое, пальмовое, какао-масло, рапсовое.
Подсолнечное масло вырабатывают из семян подсолнечника путем прессования или экстракции бензином и в зависимости от стадии очистки (рафинации) выпускают в продажу: нерафинированным, гидратированным, рафинированным недезодорированным и рафинированным дезодорированным.
Кукурузное масло получают из зародышей зерна (отделяемого при крупяном или паточном производствах) путем прессования или экстракции бензином и в зависимости от стадии очистки (рафинации) реализуют в виде: нерафинированном, рафинированном недезодорированном, рафинированном дезодорированном.
Горчичное масло изготавливается из семян горчицы путем прессования и выпускается нерафинированным, гидратированным, и рафинированным недезодорированным и дезодорированным. Жмых, остающийся после прессования, используется для получения горчичного порошка.
Хлопковое масло производят из семян хлопчатника путем прессования или экстракции бензином и в зависимости от стадии очистки (рафинации) реализуют только в рафинированном виде: нейтрализованное недезодорированное, нейтрализованное дезодорированное. Это связано с тем, что нерафинированное масло может использоваться только для технических целей, поскольку в нем содержится ядовитое вещество - госсипол. Относится к низкокачественному виду растительного масла.
Соевое масло вырабатывают из бобов сои путем прессования или экстракции бензином и в зависимости от стадии очистки (рафинации) выпускают в реализацию: нерафинированным, гидратированным, рафинированным недезодорированным, рафинированным дезодорированным.
Арахисовое масло получают из бобов арахиса путем прессования или экстракции бензином и в зависимости от стадии очистки (рафинации) реализуют в виде: нерафинированном, рафинированном недезодорированном, рафинированном дезодорированном.
Оливковое масло изготавливают из мякоти плодов оливкового дерева путем прессования или экстракции бензином
в зависимости от стадии очистки (рафинации) реализуют
в виде: нерафинированном, рафинированном недезодорированном, рафинированном дезодорированном.
Прованским маслом называют оливковое масло, полученное только путем холодного прессования (высококачественное масло, используемое в нерафинированном виде).
Деревянное масло вырабатывают путем горячего прессования жмыха, оставшегося после холодного прессования (низкокачественное оливковое масло, так же, как и экстракционное, требует дополнительной рафинации).
Кунжутное (сезамовое) масло производят из семян кунжута путем прессования и в зависимости от стадии очистки (рафинации) выпускают в виде: нерафинированном, рафинированном.
Кокосовое масло изготавливают из подсушенной и раздробленной мякоти орехов кокосовых пальм путем горячего прессования и выпускают только в рафинированном виде. При комнатной температуре имеет твердую консистенцию.
Пальмоядровое масло получают из мякоти плодов масличных пальм путем прессования и вырабатывают только рафинированным дезодорированным. Очень нестойкое при хранении масло. При комнатной температуре имеет твердую консистенцию.
Какао-масло вырабатывают из какао-бобов путем прессования и используют в основном для получения шоколада и шоколадных изделий. При комнатной температуре имеет твердую консистенцию.
Рапсовое масло производят из семян рапса путем прессования или экстракции бензином и реализуют для питания только после специальной обработки (удаление эруковой кислоты и гликозинолатов). Для переработки на пищевые продукты используется только рафинированное недезодорированное и нерафинированное масло первого сорта. Низкокачественное рапсовое масло, в основном используется для получения маргарина и кулинарных жиров.
А также жиры участвуют в производстве синтетических моющих средств весьма устойчивых и с трудом подвергаются разрушению. Поэтому они могут оказывать вредное воздействие на окружающую среду. Чтобы сточные воды очистить от синтетических моющих средств, их подвергают длительному биологическому и химическому разложению.
IV . Минеральные вещества.
IV . I . Общая характеристика.
Минеральные вещества не обладают энергетической ценностью, как белки, жиры и углеводы. Однако без них жизнь человека невозможна. Особенно важна их роль в построении костной ткани. Минеральные вещества участвуют в важнейших обменных процессах организма: водно-солевом и кислотно-щелочном. Многие ферментативные процессы в организме невозможны без участия тех или иных минеральных веществ.
Вы когда-нибудь наблюдали, как малыш увлеченно грызет кусок мела или известняка? Что это означает? Всего лишь то, что ребенок самостоятельно, доступными ему средствами, стремится пополнить в организме недостаток кальция.
Обычно минеральные вещества делят на две группы. Первая – состоит из макроэлементов, содержащихся в пище в больших количествах. К ним относят кальций, фосфор, магний, натрий, калий, хлор, серу. Вторая – состоит из микроэлементов, концентрация которых в организме невелика. В эту группу входят железо, цинк, йод, фтор, медь, марганец, кобальт, никель.
IV . II . Макроэлементы.
Кальций непосредственно участвует в самых сложных процессах, например таких, как свертывание крови, поддержание необходимого равновесия между возбуждением и торможением коры головного мозга, расщепление резервного полисахарида – гликогена, поддержание должного кислотно-щелочного равновесия внутри организма и нормальной проницаемости стенок кровеносных сосудов. Кроме того, длительный недостаток кальция в пище нежелательно сказывается на возбудимости сердечной мышцы и ритме сокращений сердца. Рацион взрослого человека должен содержать от 0,8 до 1 г кальция.
Больше всего кальция (120 мг%) содержится в молоке и молочных продуктах, например в сыре около 1000 мг% (мг% – это миллиграмм вещества на 100 г продукта, условно принимаемого за 100%). Почти 80% всей потребности в кальции удовлетворяется молочными продуктами. Однако в некоторых растительных продуктах содержатся вещества, уменьшающие всасывание кальция. К их числу относятся фитиновые кислоты в злаковых и щавелевая кислота в щавеле и шпинате. В результате взаимодействия этих кислот с кальцием образуются нерастворимые фитаты и оксалаты кальция (соли фитиновой и щавелевой кислот соответственно), которые затрудняют всасывание и усвоение этого элемента. Пища, богатая жирами, также замедляет усвоение кальция.
Среди овощей и фруктов высоким содержанием кальция отличаются фасоль, хрен, зелень петрушки, репчатый лук, урюк и курага, яблоки, сушеные персики, груши, сладкий миндаль.
При склонности организма к повышенной свертываемости крови и образованию тромбов в кровеносных сосудах количество продуктов, богатых кальцием, в рационе должно быть снижено.
Фосфор входит в состав фосфопротеидов, фосфолипидов, нуклеиновых кислот. Соединения фосфора принимают участие в важнейших процессах обмена энергии. Аденозинтрифосфорная кислота (АТФ) и креатинфосфат являются аккумуляторами энергии, с их превращениями связаны мышление и умственная деятельность, жизнеобеспеченность организма.
Потребность в фосфоре для взрослых составляет 1200 мг в день. Относительно много фосфора содержат, мг%: рыба – 250, хлеб – 200, мясо – 180, еще больше фасоль – 540, горох – 330, овсяная, перловая и гречневая крупы – 320–350, сыр – 500–600. Основное количество фосфора человек потребляет с молоком и хлебом. Обычно усваивается 50–90% фосфора. Если человек употребляет растительные продукты, то в этом случае фосфора поглощается меньше, поскольку он в значительной части находится там в виде трудно усваиваемой фитиновой кислоты.
Для правильного питания важно не только абсолютное содержание фосфора, но и соотношение его с кальцием, которое считается оптимальным для взрослого человека – 1:1,5. При избытке фосфора может происходить выведение кальция из костей, а при избытке кальция развивается мочекаменная болезнь.
Магний участвует в формировании костей, регуляции работы нервной ткани, обмене углеводов и энергетическом обмене. По данным Института питания РАМН, потребность в магнии для взрослых – 400 мг в день. Почти половина этой нормы удовлетворяется хлебом и крупяными изделиями. В хлебе содержится 85 мг% магния, овсяной крупе – 116, ячневой – 96, фасоли – 103 мг%. Из других источников питания следует отметить орехи – 170–230 мг% и большинство овощей – 10–40 мг% магния. В молоке и твороге содержится относительно мало магния – 14 и 23 мг% соответственно. Однако в отличие от растительных продуктов магний находится в них в легко усвояемой форме – в виде цитрата магния (магниевой соли лимонной кислоты). В связи с этим молочные продукты, потребляемые в значительных количествах, являются существенным источником магния для организма человека.
При нормальном питании организм, как правило, полностью обеспечивается магнием. Однако следует помнить, что избыток магния снижает усвояемость кальция. Оптимальное соотношение кальция и магния 1:0,5, что обеспечивается обычным подбором пищевых продуктов. При этом следует учитывать, что больше всего магния содержат продукты растительного происхождения, особенно пшеничные отруби, соевая мука, сладкий миндаль, горох, пшеница, абрикосы, белокочанная капуста.
Натрий участвует в образовании желудочного сока, регулирует выделение почками многих продуктов обмена веществ, активирует ряд ферментов слюнных желез и поджелудочной железы, а также более чем на 30% обеспечивает щелочные резервы плазмы крови. Кроме того, ионы натрия способствуют набуханию коллоидов тканей, это задерживает воду в организме.
4–6 г в день, в том числе около 2,4 г натрия с хлебом и 1–3 г при подсаливании пищи. Основное количество натрия – около 80% – организм получает при поглощении продуктов с добавлением поваренной соли.
В древности человек не добавлял соль в пищу. Поваренную соль в питании начали использовать примерно в последние две тысячи лет, сначала как вкусовую приправу, а затем и как консервирующее средство. Однако до сих пор многие народности Африки, Азии и Севера прекрасно обходятся без пищевой соли.
Потребность в натрии существует, но она невелика – около 1 г в день и в основном удовлетворяется обычной диетой без добавления пищевой соли (0,8 г в день). Однако потребность в этом макроэлементе существенно возрастает при сильном потоотделении в жарком климате или при больших физических нагрузках. Вместе с тем установлена прямая зависимость между избыточным потреблением натрия и гипертонией. С наличием натрия в организме связывают также способность тканей удерживать воду. В связи с этим избыточное потребление поваренной соли перегружает почки; при этом страдает и сердце. Вот почему при заболеваниях почек и сердца рекомендуется резко ограничить потребление соли. Для большинства людей совершенно безвредно 4 г натрия в день. Другими словами, помимо 0,8 г естественного натрия можно потреблять еще 3,2 г натрия, т. е. 8 г поваренной соли.
Калий – внутриклеточный элемент, регулирующий кислотно-щелочное равновесие крови; участвует в передаче нервных импульсов и активирует работу ряда ферментов. Считается, что калий обладает защитным действием против нежелательного действия избытка натрия и нормализует давление крови. По этой причине в некоторых странах предложено выпускать поваренную соль с добавлением хлорида калия.
В большинстве продуктов содержание калия колеблется в пределах 150–170 мг%. Заметно больше его лишь в бобовых, например в горохе – 870, фасоли – 1100 мг%. Много калия содержится в картофеле – 570, яблоках и винограде – около 250 мг%.
Ежедневная потребность взрослого человека в калии составляет 2500–5000 мг и удовлетворяется обычным рационом за счет картофеля, которого в нашей стране потребляется относительно много.
Хлор участвует в образовании желудочного сока, формировании плазмы; активирует ряд ферментов. Естественное содержание хлора в пищевых продуктах колеблется в пределах 2–160 мг%. Рацион без добавления поваренной соли содержал бы около 1,6 г хлора. Основное его количество (до 90%) взрослые получают с поваренной солью.
Потребность в хлоре (около 2 г в день) с избытком удовлетворяется обычным рационом, содержащим 7–10 г хлора; из них около 4 г мы получаем с хлебом и 1,5–4,6 г при подсаливании пищи поваренной солью.
Кроме того, малосоленая пища полезна при заболеваниях поджелудочной железы, печени и желчевыводящих путей, некоторых болезнях желудка, а также в тех случаях, когда в лечебно-профилактических целях назначаются гормональные препараты.
Сера в организме человека – непременная составная часть клеток, ферментов, гормонов, в частности инсулина, вырабатываемого поджелудочной железой, и серосодержащих аминокислот. Довольно много ее в нервной, соединительной и костной тканях. Считается, что суточный пищевой рацион взрослого здорового человека должен содержать 4–5 г серы. Такое ее количество обычно обеспечивает правильно организованное питание, которое включает мясо, куриное яйцо, овсяную и гречневую крупы, хлебобулочные изделия, молоко, сыры, бобовые и капусту.
IV . III . Микроэлементы.
Железо незаменимо в процессах кроветворения и внутриклеточного обмена. Примерно 55% железа входит в состав гемоглобина эритроцитов, около 24% участвует в формировании красящего вещества мышц (миоглобина), примерно 21% откладывается «про запас» в печени и селезенке. Суточная потребность взрослого здорового человека в железе составляет 10–20 мг и восполняется обычным сбалансированным питанием. Однако следует учитывать, что при использовании в пище хлеба из муки тонкого помола, содержащей мало железа, у городских жителей весьма часто наблюдается дефицит железа. Обращает на себя внимание тот факт, что зерновые продукты, богатые фосфатами и фитином, образуют с железом труднорастворимые соли и снижают его усвояемость организмом. Так, если из мясных продуктов усваивается около 30% железа, то из зерновых – не более 10%. Чай также снижает усвояемость железа из-за связывания его с дубильными веществами с образованием труднорасщепляемого комплекса. Люди, страдающие железодефицитной анемией, должны поэтому употреблять больше мяса и не злоупотреблять чаем.
Наиболее богаты железом сушеные белые грибы, печень и почки убойного скота, персики, абрикосы, рожь, зелень петрушки, картофель, репчатый лук, тыква, свекла, яблоки, айва, груши, фасоль, чечевица, горох, толокно, куриное яйцо, шпинат.
Цинк – элемент, значение которого определяется тем, что он входит в состав гормона инсулина, участвующего в углеводном обмене, и многих важных ферментов, обеспечивающих должное течение окислительно-восстановительных процессов и тканевого дыхания. Специфические последствия длительного недостатка цинка в пище – это прежде всего снижение функции половых желез и гипофиза головного мозга. Чтобы этого не случилось, взрослый здоровый человек должен ежедневно получать с пищей 10–15 мг цинка, которого больше всего в мясе гусей, фасоли, горохе, кукурузе, говядине, свинине, курице, рыбе, говяжьей печени, а также в молоке, яблоках, груше, сливе, вишне, картофеле, капусте, свекле и моркови.
Йод является необходимым элементом, участвующим в выработке щитовидной железой гормона тироксина, поэтому почти половина его концентрируется именно в этой железе. При длительном недостатке йода в пище развивается зобная болезнь (тиреотоксикоз). Особенно чувствительны к недостатку йода дети школьного возраста. Потребность в нем колеблется в пределах 100–150 мкг в день. Содержание йода в пищевых продуктах обычно невелико – 4–15 мкг%. Однако в морской рыбе его содержится около 50 мкг%, печени трески – до 800, морской капусте в зависимости от вида и сроков сбора – от 50 до 70 000 мкг%. Следует учитывать, что при длительном хранении или тепловой обработке пищи теряется от 20 до 80% этого микроэлемента.
25 мг на 1 кг соли. Однако срок хранения такой соли всего полгода, поскольку йод при хранении соли постепенно улетучивается.
Фтор – элемент, при недостатке которого развивается такая болезнь зубов, как кариес, приводящая к разрушению зубной эмали. Потребность в нем взрослого человека составляет 3 мг в день. При этом одну треть фтора человек получает с пищей и две третьих – с водой. В пищевых продуктах фтора обычно содержится мало. Исключение составляет морская рыба – в среднем 500 мг%, при этом в скумбрии содержится до 1400 мг%.
В районах, где фтора в воде меньше 0,5 мг/л, производят ее фторирование. Однако избыточное потребление фтора также нежелательно, поскольку вызывает флуороз, выражающийся в пятнистости зубной эмали.
Медь необходима для регулирования процессов снабжения клеток кислородом, образования гемоглобина и «созревания» эритроцитов. Она также способствует более полной утилизации организмом белков, углеводов и повышению активности инсулина. Для осуществления всех этих процессов здоровому человеку необходимо 2 мг меди, которая, как правило, содержится в рационе, включающем горох, овощи и плоды, мясо, хлебобулочные изделия, рыбу. Считается также, что 1 л питьевой воды содержит 1 мг меди. Больше всего ее в печени убойных животных.
Марганец активно влияет на обмен белков, углеводов и жиров. Важной также считается способность марганца усиливать действие инсулина и поддерживать определенный уровень холестерина в крови. В присутствии марганца организм полнее использует жиры. Сравнительно богаты этим микроэлементом крупы (в первую очередь овсяная и гречневая), фасоль, горох, говяжья печень и многие хлебобулочные изделия, которыми практически восполняется суточная потребность человека в марганце – 5,0–10,0 мг.
Кобальт находится в составе витамина В 12 (кобаламин), содержащего его около 4,5%. При недостаточном потреблении кобальта проявляются некоторые нарушения функции центральной нервной системы, малокровие, снижение аппетита.
Кобальт способен избирательно угнетать дыхание клеток злокачественных опухолей и тем самым, конечно, их размножение. Другим специфическим достоинством кобальта считают его способность в два–четыре раза интенсифицировать противомикробные свойства пенициллина. Больше всего кобальта содержат говядина, виноград, редис, салат, шпинат, свежий огурец, черная смородина, клюква, репчатый лук, говяжья и особенно телячья печень. В сутки человек должен поглощать с пищей 0,1–0,2 мг кобальта.
Никель в сочетании с кобальтом, железом, медью также участвует в процессах кроветворения, а самостоятельно – в обмене жиров, обеспечении клеток кислородом. В определенных дозах никель активизирует действие инсулина. Потребность в никеле вполне обеспечивается рациональным питанием, содержащим, в частности, мясо, овощи, рыбу, хлебобулочные изделия, молоко, фрукты и ягоды.
Заключение .
Таким образом, белки, жиры, углеводы являются неотъемлемой частью живого организма, а также необходимость поступления их в организм человека. Их сложное строение дает представление о сложном химическом составе продуктов питания, употребляемые человеком, а также их сложное строение дает различные функции клетки. Не остались в стороне и минеральные вещества: макро- и микроэлементы. Они позволяют достраивать сложные молекулы органических веществ, а также являются строительным материалом организма.
Список литературы.
1. В.П. Комов, В.Н. Шведова. Биохимия. М: Дрофа, 2004. – с.28-47, 52-59, 222-237, 284-300.
2. Г.Е. Рудзитис, Ф.Г. Фельдман. Химия 10. М: Просвещение, 1993. – с.117-134.
3. Г.Е. Рудзитис, Ф.Г. Фельдман. Химия 11. М: Просвещение, 1997.
4. А.И.Артеменко, И.В. Тикунова. Химия 10-11. М: Просвещение, 1993.
